3Q 누적 매출 0.4%↑, 영업익 43.4%↓···영업익은 기저효과로 감소, 판관비율 유지
스텔라라 시밀러 ‘DMB-3115’, 내년 하반기 허가 결정···허가 시 유럽 시장 안착 여부 주목
그로트로핀, 장기지속형 주사제 개발 검토···과민성방광약 ‘DA-8010’ 임상도 내년 초 종료 예상
[시사저널e=이상구 의약전문기자] 동아에스티는 올해 실적과 수치상으로는 다소 부진한 해를 보냈다. 하지만 내년에는 그동안 진행했던 바이오시밀러(복제약) 허가와 출시가 예상되는 등 반등 가능성이 예고된다.
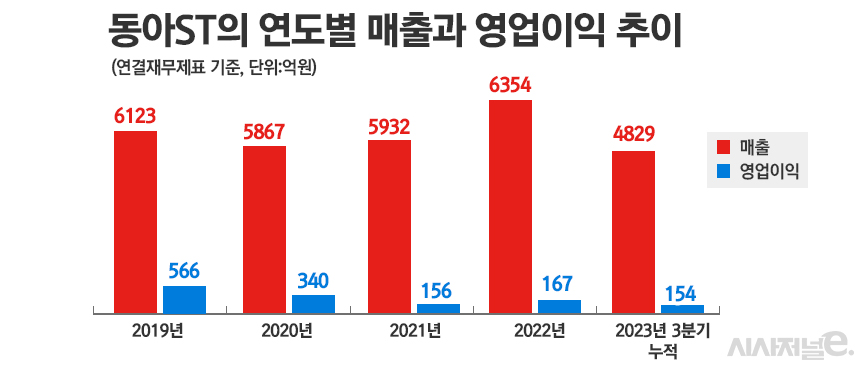
11일 관련업계에 따르면 동아에스티는 연결재무제표 기준 올 3분기 누적 4829억원 매출을 올려 지난해 같은 기간에 비해 0.4% 성장했다. 반면 영업이익은 154억원을 기록하며 전년대비 43.4% 하락했다. 영업이익의 경우 지난해 해외사업부문과 의료기기, 진단사업 부문이 고르게 성장한 기저효과로 감소했다는 회사측 설명이다. 반면 성장호르몬제 ‘그로트로핀’ 급성장이 매출원가율 부진을 막는데 영향을 줬고 전년대비 R&D(연구개발) 비용이 늘지 않았으며 판매관리비가 효율화됐다는 것이 동아에스티 입장이다.
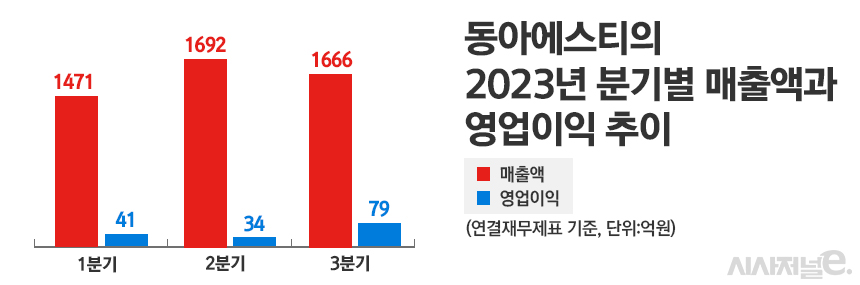
실제 동아에스티가 자체 개발한 그로트로핀은 3분기에만 258억원 매출을 올려 전년대비 59.3% 성장했다. 앞서 1분기와 2분기 모두 200억원을 넘는 실적을 달성한 것으로 파악된다. 그로트로핀은 동아에스티가 자체적으로 개발한 품목인 만큼 매출원가비율에 긍정적 여파를 주게 된다. 올해 최소 900억원이 넘을 것으로 예상되는 그로트로핀 성장은 동아에스티 매출원가율이 지난해 50.4%에서 올해 50.8%로 소폭 올라가는데 영향을 줬다는 분석이 가능하다. 회사 R&D 비용은 지난해 841억원에서 올해 821억원으로 20억원 감소했다. 판관비율은 지난해와 올해 31.6%로 동일했다.
바이오의약품 그로트로핀은 뇌하수체 성장호르몬 분비장애로 인한 소아의 성장부전, 터너증후군으로 인한 성장부전, 임신수주에 비해 작게 태어난 저신장 소아에서의 성장장애 적응증, 특발성 저신장증에 대한 적응증을 갖고 있다. 현재 장기지속형 주사제 개발을 검토하고 있어 주목된다. 제약업계 관계자 A씨는 “동아에스티는 발매 이후 환자 편의를 위해 그로트로핀 동결건조제를 액상형제로 바꾸고 펜타입 제형을 추가로 내놨는데 장기지속형 주사제 개발에 성공하면 시장 판도가 달라질 수 있다”고 예상했다.
이같은 올해 실적과 달리 동아에스티는 그동안 꾸준히 진행한 R&D(연구개발)를 통해 2024년 매출이 성장할 토대를 마련했다는 업계 분석이다. 우선 동아에스티가 지난 2013년부터 메이지세이카파마와 공동 개발해 온 ‘스텔라라’ 바이오시밀러(복제약) ‘DMB-3115’ 매출이 내년부터 발생할 전망이다. 글로벌 임상 3상에서 오리지널 스텔라라와 치료적 동등성을 입증한 DMB-3115는 지난 6월 유럽의약품청 허가 신청을 완료한 상태다. 이에 내년 하반기에는 DMB-3115의 유럽 허가 여부가 결정될 것으로 예상된다.
미국 시장의 경우 조만간 미국 FDA(식품의약국)에 허가를 신청할 예정이어서 내년 내로 진입 여부가 결정될 가능성이 예상된다. 스텔라라는 지난해 97억 2000만달러(12조 7600억원) 매출을 기록한 블록버스터 품목이어서 바이오시밀러 유럽 허가와 출시가 확정될 경우 동아에스티 매출에 직접 반영될 것으로 전망된다. 참고로 동아에스티는 한국 식품의약품안전처에는 DMB-3115 허가를 신청하지 않은 것으로 파악됐다.
동아에스티는 과민성방광 치료제 ‘DA-8010’ 임상 3상도 진행 중이다. 기존 항무스카린제 대비 우수한 방광 자발 수축 억제 효능 및 방광 선택성으로 부작용 구갈, 변비 및 유효성을 개선한 치료제로 개발하고 있다는 회사측 설명이다. DA-8010은 동아에스티가 지난 2010년 개발을 시작한 품목이어서 예상대로 2024년 초 임상 3상을 마무리할 경우 14년을 투자한 사례로 꼽힐 전망이다. 제약업계 관계자 B씨는 “글로벌 과민성방광 치료제 시장은 42억 달러 규모로 추산되는데 국내에서도 제일약품이 신약 ‘베오바’를 출시한 상황에서 동아에스티가 임상 3상을 완료하면 업계 관심이 집중될 것”으로 전망했다.
이밖에도 동아에스티는 비만치료제 신약후보물질 ‘DA-1726’에 대한 글로벌 임상 1상 진행을 위해 FDA에 임상시험계획을 신청할 예정이다. 결국 동아에스티는 내년 바이오시밀러 DMB-3115 유럽 허가와 함께 바이오의약품 그로트로핀 매출 증대에 기대를 걸고 있다. 이와 함께 과민성방광 치료제 임상 3상 종료가 예상되는 상황에서 실적 추이가 어떻게 진행될지 주목된다.
제약업계 관계자 C씨는 “전통제약사 동아에스티가 나름대로 바이오의약품에 공을 들였는데 구체적 성과가 나오는 시점이 2024년으로 예상된다”며 “내년 최대 이슈는 DMB-3115가 유럽시장에 안착할 수 있느냐로 판단된다”고 말했다.

