4월 ‘자큐보’ 37호 허가···‘티굴릭소스타트’는 내년 임상 종료, DA-0810은 유효성 입증 실패
작년 11월 신청 어나프라는 올해 내 결정 가능성···업계 “허가 획득 후 비급여 출시” 예상
국내 비마약성 진통제는 경증만 사용, 1200억대 규모···어나프라, 중등도 이상 환자에 활용
[시사저널e=이상구 의약전문기자] 올해 안으로 국산신약 38호 의약품이 나올 지 주목된다. 현재로선 후보군 중 비보존제약의 비마악성 진통제 ‘어나프라’가 앞선 상태여서 업계 관심이 쏠리고 있다.
25일 관련업계에 따르면 제일약품 자회사인 온코닉테라퓨틱스 ‘자큐보정’이 지난 4월 식품의약품안전처로부터 국내개발신약 37호 품목허가를 받은 이후 국산신약 배출이 5개월간 중단된 상태다. 이에 임상 과정과 허가 신청 등을 기준으로 비보존제약 어나프라(성분명 오피란제린)와 LG화학 통풍 치료제 ‘티굴릭소스타트’, 동아에스티의 과민성 방광 치료제 ‘DA-0810’이 그동안 국산신약 38호 후보로 거론돼왔다.
이중 어나프라의 경우 지난해 11월 식약처에 허가를 신청했기 때문에 가장 앞서 있는 상태다. 반면 티굴릭소스타트는 2025년 12월 임상 3상이 종료될 예정이고 2026년 허가 신청, 2027년 허가 승인, 2028년 판매 본격화라는 일정을 LG화학이 제시했다. 동아에스티 DA-0810은 임상 3상에서 유효성 입증에 실패한 후 추가 유효성 분석 및 하위그룹 분석을 진행 중이다.
현 시점에서 국산신약 38호로 유력한 어나프라에 대해 비보존제약 관계자 A씨는 “지난해 허가를 신청했고 식약처 검토 기간이 1년인 점 등을 감안하면 허가 여부가 결정되는 시점은 올해 말 정도로 예상된다”고 말했다. 관행적으로 식약처의 신약 허가 과정은 안전성과 유효성 검사가 마무리되면 GMP(의약품 제조 및 품질관리기준) 실사를 진행하게 된다. 비보존제약은 안유검사 종료와 GMP 실사 착수 여부에 대한 확인을 유보하고 허가 심사가 원활하게 진행된다는 점만 밝혔다. 제약업계 관계자 B씨는 “허가 과정에서 안유검사가 끝나면 80%가 마무리된 셈”이라며 “통상 GMP 실사는 보완이 가능하다”고 설명했다.
만약 비보존제약이 어나프라 허가를 획득할 경우 급여와 비급여 중 어느 선택을 할 지도 업계 관심사다. 현행 제도상 급여 작업을 진행하려면 5-6개월이 소요될 가능성이 있는데 이를 포기하고 비급여를 결정하면 즉시 출시가 가능한 상황이다. 이에 대해 비보존제약은 여러 가지 선택지를 폭넓게 논의하는 상황이라고 답변했다. 비보존제약 동향에 정통한 제약업계 관계자 C씨는 “비보존은 현재 어나프라 급여와 관련된 구체적 준비 대신 마케팅 본부 운영 등 사전 마케팅에 주력하고 있어 비급여를 선택할 가능성이 높다”고 말했다. 어나프라 허가를 받는 대로 즉시 비급여 출시해 시장 평가를 받을 것으로 예상한다는 설명이다.
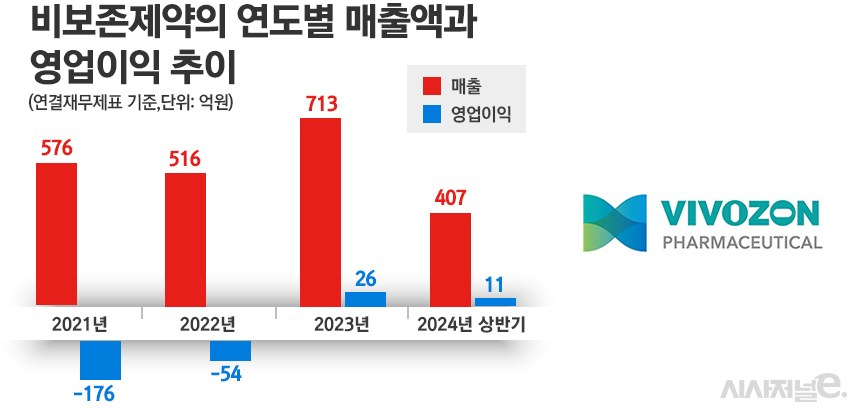
이처럼 허가 과정에서부터 업계가 주목하는 것은 그만큼 비보존제약이 어나프라 출시에 공을 들이고 있기 때문으로 분석된다. 어나프라는 비보존이 개발한 계열 내 최초 비마약성 진통제다. 비보존은 수술 후 통증 치료 1차 치료제로서 마약성 진통제를 대체할 수 있는 의약품으로 어나프라를 개발했다. 임상 3상을 마무리한 비보존제약은 지난해 5월 어나프라 허가를 위한 신속심사 지정 신청서를 제출했다가 철회하고 8월 사전검토와 11월 허가를 잇달아 신청하는 등 우여곡절을 경험하기도 했다.
제약업계 관계자 D씨는 “국내에서 비마약성 진통제 특히 중등도 이상 통증으로는 허가를 신청한 제약사가 없었기 때문에 비보존제약은 물론 식약처도 생소했던 상황”이라고 전했다. 핵심은 현재 국내 출시된 비마약성 진통제는 강도가 비교적 낮은 경증 통증에만 사용된다는 점이다. 수술 후 통증을 비롯한 신경병성 통증 등 중등도 이상 통증에 사용할 비마약성 진통제가 부재한 상황에서 어나프라 허가가 확정될 경우 그 여파가 클 것으로 전망된다.
제약업계 관계자 E씨는 “비마약성 진통제 시장의 경우 글로벌은 2030년 기준 100조원 규모를 형성할 전망이고 국내는 1200억원대 규모로 추산된다”며 “어나프라가 마약성 진통제를 대체할 수 있다고 판단하고 있어 향후 시장은 더욱 커질 것”으로 예상했다. 결국 비보존제약 어나프라 허가 여부가 올해 안으로 결정될 가능성이 높은 것으로 관측된다. 만약 허가가 결정되면 비보존이 비급여 출시할지 주목된다.
