에스티팜, 지난해 사상 최대 실적 달성
올리고핵산 원료 CDMO 전체 실적 견인
신약 R&D 성과는 지지부진···업계 '회의적'
[시사저널e=최다은 기자] 에스티팜이 올리고핵산치료제 CDMO(위탁개발생산)로 매년 수익성을 강화하며 호실적을 이어가고 있다. 다만 신약 개발에서는 주목할만한 성과를 내지 못하고 있다. 일각에서는 연구 성과에 대한 회의적인 반응도 나온다.
19일 업계에 따르면 에스티팜은 지난해 올리고핵산 원료 수요 증가에 힘입어 역대 최대 실적을 달성했다. 에스티팜의 올리고뉴클레오타이드 CDMO는 올리고뉴클레오타이드의 만성질환 영역에서의 사용 확장되면서 전 세계적으로 수요가 증가하는 추세다.
올리고는 DNA와 RNA를 구성하는 분자인 뉴클레오타이드를 여러개 결합한 고분자 물질이다. 주로 RNA 치료제 원료로 사용되고 있다. 에스티팜은 올리고뉴클레오타이드 제조 CDMO 아시아 1위, 글로벌 3위에 안착하며 경쟁력을 높이고 있다.
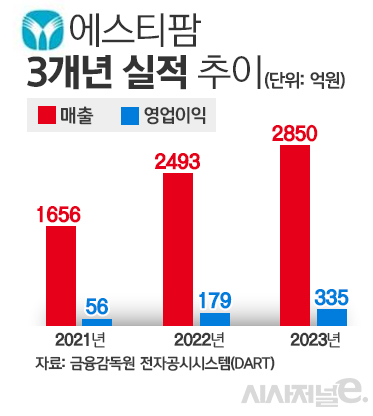
◇ 올리고 CDMO, 사상 최대 실적 견인
에스티팜은 지난해 매출과 영업이익이 각각 2850억원, 335억원을 기록했다. 전년 대비 14%, 87.3% 증가한 수치다. 특히 영업이익은 2021년 56억원과 비교해 2년 만에 6배가량 늘어나면서 수익성이 대폭 강화됐다.
에스티팜은 동아쏘시오그룹의 원료의약품(API) CDMO(위탁개발생산) 계열사다. 올리고핵산치료제 제조 CDMO로 사업을 확장하고 있다. 에스티팜의 실적 호조는 올리고뉴클레오타이드 CDMO 사업 매출액이 늘어나면서 전체 실적을 견인했다. 사업별 매출 현황을 살펴보면, 가장 많은 비중을 차지하는 올리고뉴클레오타이드 사업이 1696억원(59.7%), 제네릭 사업 496억원(17.5%), CRO 등 기타 사업이 336억원(11.8%), 저분자(Small Molecule) 사업 217억원(7.6%), mRNA 사업 94억원(3.3%)을 차지한다.
항체-약물 접합체(ADC) 분야와 글로벌 기업의 신약 승인도 새로운 성장 모멘텀이 될 전망이다. 에스티팜은 미국 바이오 기업 '제론'에 골수형성이상증후군(MDS) 리보핵산(RNA) 치료제 '이메텔스타트' 임상 물량을 공급하고 있다. 이메텔스타트의 미국 식품의약국(FDA) 신약 승인 기대감이 높아지면서, 에스티팜의 수혜가 예상된다.
제론은 이달 14일 FDA 항암제자문위원회(ODAC)가 해당 제품의 임상 유효성을 검토해 12대 2로 찬성했다고 전했다. 신약 승인 여부는 오는 6월 최종 결정된다. 권해순 유진투자증권 연구원은 리포트를 통해 “FDA가 이메텔스타트를 승인할 가능성이 매우 높다고 판단된다”며 “만약 승인되면 올 하반기부터 에스티팜은 해당 약의 상업화 물량을 생산할 예정”이라고 설명했다.
에스티팜은 CDMO 생산 파이프라인 다각화에도 속도를 내고 있다. 이달 레고켐바이오와 ADC 링커 제조공정 공동 연구 및 제조 위탁계약을 체결했다. CDMO 포트폴리오를 ADC 분야로 확장한다고 알렸다.

◇ 10년째 신약 글로벌 기술이전 無
그러나 신약 개발에서는 다소 지지부진한 성적을 내고 있다. 에스티팜은 동아쏘시오그룹 자회사로 합류한 이후 주목할만한 글로벌 기술이전 성과를 내지 못하고 있다. 지난 2021년 11월 비알코올성 지방간염(NASH) 치료제를 국내 바이오텍에 기술이전한 것이 전부다. 최근에는 파이프라인 간소화를 단행했다. 핵심 파이프라인 중 임상 2상 단계에 진입한 신약이 1개 밖에 없다는 것도 한계점으로 지적된다.
에스티팜은 지난 2010년 동아쏘시오그룹으로 편입한 이후 2011년부터 신약 개발에 뛰어들었다. 2013년 에이즈 치료제 개발을 본격화하면서 신약 연구 역량을 키워왔다. 신약후보물질 기술수출 시, 원료의약품 공급 계약을 함께 맺는 등 CDMO 사업과 시너지를 내겠다는 복안이다. 에스티팜은 임상 2상 단계 이후 기술수출을 추진하는 전략으로 연구개발을 지속하고 있다.
에스티팜이 보유한 인체 대상 임상시험에 진입한 파이프라인은 총 3개다. 계열 내 최초(First-in-class) 신약으로 개발 중인 에이즈 치료제 ‘STP0404’와 항암제 ‘STP1002’, 코로나19 mRNA 백신 ‘STP2104’가 해당된다. 위 세 가지 신약 중 임상 2상 단계에 도달한 파이프라인은 에이즈 치료제 STP0404 뿐이다.
가장 개발 진도가 빠른 에이즈 치료제 STP0404는 지난해 5월 미국에서 임상 2a상 첫 환자 투약을 시작했다. 올해 상반기 2a상 종료될 예정이다. 3분기 중에 중간결과 발표가 예상된다. 항암제로 개발 중인 STP1002은 올해 상반기 임상 1상 결과가 나올 것으로 기대된다. 코로나19 mRNA 백신 STP2104는 남아공과 국내에서 임상 1상을 완료했다.
다만 코로나19 mRNA 백신 STP2104는 엔데믹 이후 코로나19 백신에 대한 시장성이 꺾이면서 투자 매력도가 떨어졌다는 평가가 지배적이다. 실제 코로나19 백신을 개발해오던 수십 곳의 국내 업체들은 개발 중단과 포기를 결정한 바 있다. 모두 상업화 이후 사업성이 없다는 이유에서다. 에스티팜 역시 새 변이종에 대응할 수 있는 범코로나 백신 후보물질인 ‘STP2250’에 대해 지난해 2월 국내에서 임상1·2a상 신청했지만, 상업성이 없다고 판단해 임상시험을 자진 취소했다.
항암제로 개발 중인 STP1002는 2015년부터 연구를 시작해 개발 10년 차에 접어들었지만, 미국 1상 환자 투약까지만 완료한 상태다. 지난해 1상 결과 발표가 예상됐지만, 올해로 미뤄졌다.
에스티팜 관계자는 “에이즈 치료제 STP0404는 기존 에이즈 치료제의 내성을 극복할 수 있는 신약으로 개발 중”이라며 “STP0404 임상 2a상 이후 기술이전 전략은 아직 공개하기 어려운 단계”라고 말을 아꼈다.

