연간 3400억대 매출규모 추산, 작년 3Q 2311억···5개 성분 1위는 다국적 제약사 오리지널
프레가발린 1위 ‘리리카’, ‘카발린’과 차이 커···레비티라세탐 ‘케프라’도 제네릭과 비교 안 돼
가바펜틴 제제 ‘뉴론틴’은 시장 독주···‘세노바메이트’는 허가 준비, “국내 유통 시 변화 예상”
[시사저널e=이상구 의약전문기자] 연간 3400억원대로 추산되는 국내 뇌전증 치료제 시장에서 SK바이오팜 ‘세노바메이트’가 출시될 경우 다국적 제약사가 매출 1위를 기록하는 구조가 변경될 지 주목된다.
23일 관련업계에 따르면 국내 뇌전증 치료제 시장은 연간 3400억원대로 추산된다. 시사저널e가 제약사들로부터 입수한 의약품 시장조사 전문기관 ‘아이큐비아’ 자료에 따르면 뇌전증 치료제 시장 주요 5개 성분의 2023년 매출은 3356억원으로 집계됐다. 2024년 3분기 누적 매출은 2311억원이다.
과거 ‘간질’로도 불리웠던 뇌전증은 치매, 뇌졸중과 함께 3대 뇌질환으로 꼽히고 있다. 구체적으로 1세대 치료제 ‘카바마제핀’, ‘페니토인’ 등 나트륨통로 억제제에 이어 2세대 치료제 ‘조니사미드’, ‘가바펜틴’, ‘프레가발린’, ‘라모트리진’, 최근 등장한 3세대 치료제 ‘라코사미드’, ‘세노바메이트’, ‘브리바라세탐’, ‘페람파넬’, ‘에스리카바제핀’, ‘루피나미드’ 등으로 구분된다.
자료에는 연매출 1200억원대인 ‘프레가발린’ 제제와 ‘레비티라세탐’ 제제, ‘가바펜틴’ 제제, ‘토피라메이트’ 제제, ‘라모트리진’ 제제의 2023년과 2024년 3분기 매출이 포함됐다. 5개 성분 공통점은 다국적 제약사가 매출 1위를 점유했으며 2위부터 국내 제약사 제네릭(복제약) 품목이 점유한 상황이다. 특히 1위와 2위 매출이 큰 차이를 보인 점이 눈길을 끌었다. 제약업계 관계자 A씨는 “5개 성분만 봤을 때 모두 다국적 제약사가 1위를 기록했으며 2위 이하 국내 제약사와 금액 갭이 큰 것은 국내 뇌전증 치료제 시장을 다국적 제약사가 점유했다는 방증”이라고 분석했다.
실제 프레가발린 제제 1위와 2위는 각각 ‘비아트리스코리아’ ‘리리카’와 HK이노엔 ‘카발린’이다. 리리카의 2023년과 2024년 3분기 매출은 각각 606억원과 423억원이다. 업계에 따르면 리리카의 지난해 원외처방금액은 700억원을 넘는 것으로 알려졌다. 반면 카발린 매출은 2023년 113억원, 2024년 3분기 86억원으로 파악돼 차이를 좁히기 쉽지 않은 상황이다. 제약업계 관계자 B씨는 “프레가발린의 경우 유한양행 등 일부 국내 제약사가 서방정 품목을 출시, 경쟁하는 상황”이라며 “중등증 신장애 환자에 사용 가능한 품목 특성상 시장 동향은 섣불리 언급하기 힘들다”고 말했다.
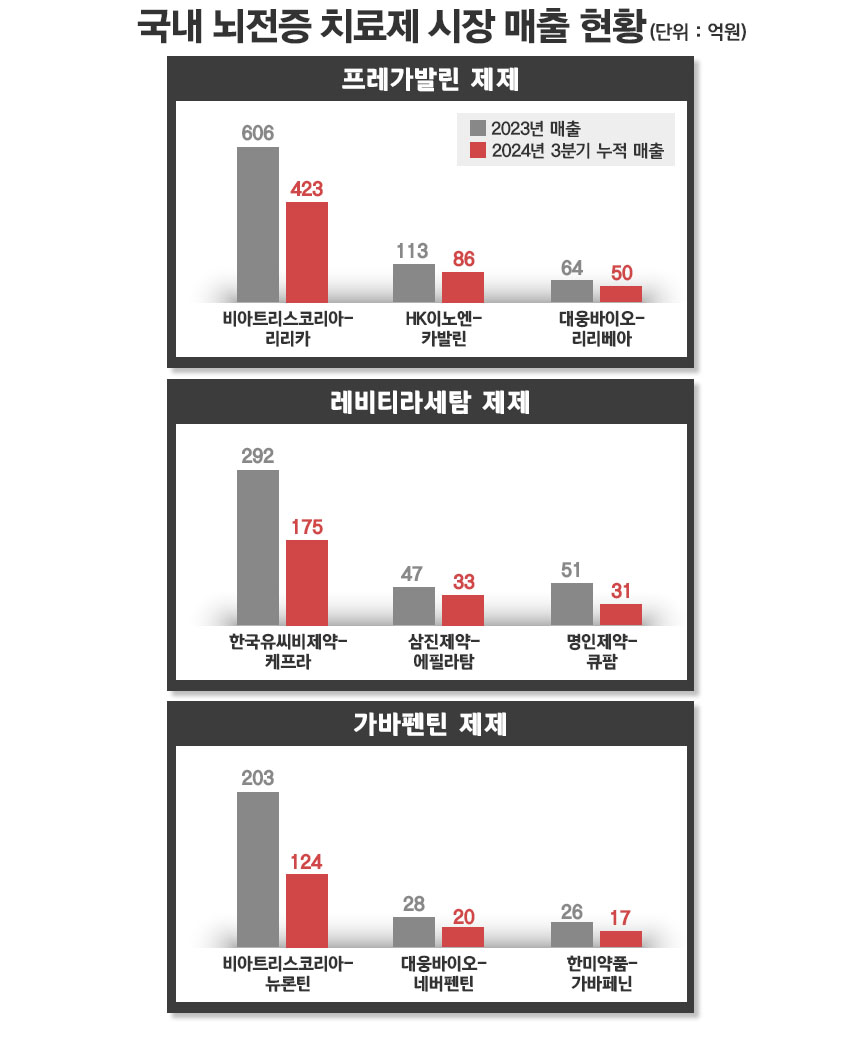
레비티라세탐 제제는 한국유씨비제약 ‘케프라’가 1위를 달리고 있다. 2023년과 2024년 3분기 매출이 각각 292억원과 175억원으로 확인됐다. 한국유씨비 ‘케프라엑스알’도 순위권에 포진해 있다. 삼진제약과 명인제약, 셀트리온제약 등 국내사들이 뒤를 쫓고 있다. 제약업계 관계자 C씨는 “삼진제약은 ‘에필라탐’에 이어 2022년 4월 에필라탐서방정500mg과 에필라탐서방정750mg를 출시하며 속효정과 서방정 시장을 동시 노렸다”며 “오리지널 품목과 차이가 있지만 국내 제약사 중에서는 앞서 있다”고 말했다.
가바펜틴 제제 매출 1위는 비아트리스코리아 ‘뉴론틴’이다. 매출은 2023년 203억원, 2024년 3분기 124억원이다. 대웅바이오 등 4개 제약사 후발의약품은 상대적으로 매출규모가 작은 상황이다. 제약업계 관계자 D씨는 “가바펜틴 제제 역시 일부 국내 업체들이 서방정 품목을 내놓으면서 도전하는데 시장 상황을 지켜보고 있다”며 “가바펜틴 속효정에 비해 서방정 적응증이 적다는 것도 참고사항”이라고 말했다.
이처럼 5개 성분 중심 뇌전증 치료제 시장 비중이 다국적 제약사에 쏠려 있는 현실에서 SK바이오팜 세노바메이트 출시 준비 상황이 주목된다. 세노바메이트는 지난 2019년 11월 미국 FDA(식품의약국) 허가를 획득한 후 2020년 5월 미국에서 출시됐다. 이어 5개 대륙에 진출한 상황이지만 국내에서는 식품의약품안전처에 허가를 신청하지 못한 상태다. SK바이오팜으로부터 국내 시장 판권을 확보한 동아에스티는 현재 허가 신청을 준비하고 있다고 밝혔다.
제약업계 관계자 E씨는 “올해부터 식약처가 허가 신청 비용을 올리며 심사 기간 단축을 선언했기 때문에 기존 1년여 기간이 줄어들 가능성이 높다”며 “SK바이오팜 세노바메이트가 국내에 유통되면 큰 변화가 있을 것으로 예상된다”고 말했다. 익명을 요청한 환자단체 관계자 F씨도 “세노바메이트를 기다리는 환자들이 적지 않은 것으로 알고 있다”며 “조속한 허가 등 행정 절차를 거쳐 국내 환자들도 신약 혜택을 받도록 해야 한다”고 말했다.
