6월 YP-P10 임상 결과 발표 후 보류 상태···개발 어려움 등 여러 요인 감안한 듯
두타스테리드 성분 ‘아보다트’ 크기 줄인 개량신약 추진···미국과 유럽 겨냥, 내년 임상 개시
[시사저널e=이상구 의약전문기자] 그동안 안구건조증 치료 신약을 개발해왔던 유유제약이 이를 보류한 것으로 파악됐다. 대신 유유제약은 ‘두타스테리드’ 성분의 탈모 치료제 개발을 추진하고 있어 향후 추이가 주목된다.
31일 관련업계에 따르면 중견 제약사인 유유제약은 안구건조증 치료제 ‘YP-P10’의 미국 임상 1/2상 시험 결과를 지난 6월 발표했다. YP-P10은 임상 1/2상 투약 종료 시점인 12주차에 접어들수록 1차 평가 지표인 TCSS(총각막염색지수)와 ODS(안구불편감)가 개선되는 추세를 보였지만 위약군 대비 통계적으로 유의미한 차이를 찾을 수 없었다. 이에 유유제약은 신약개발 자문단과 함께 YP-P10 임상 결과를 분석한 후 R&D(연구개발) 방향을 수립할 계획이라고 밝힌 바 있다.
유유제약에 따르면 현재 YP-P10 개발을 보류한 상태다. 임상을 통해 YP-P10 안전성에 대한 긍정 데이터와 내약성이 일부 확인된 상태에서 개발을 포기할 수 없는 반면 여러 현실적 사유로 인해 강행도 부담스러운 입장으로 분석된다. 우선 안구건조증 치료제 개발은 다른 치료제에 비해 어려운 분야로 꼽힌다. 안구건조증은 과도한 눈물 증발이나 수분 부족으로 안구 표면이 손상되면서 발생하는 질환이다. 전 세계 치료제 시장규모는 오는 2027년 65억 달러대로 성장할 전망이다. 이같은 규모 때문에 개발에 나서는 업체는 많지만 성공 사례는 극히 드문 것으로 파악된다.
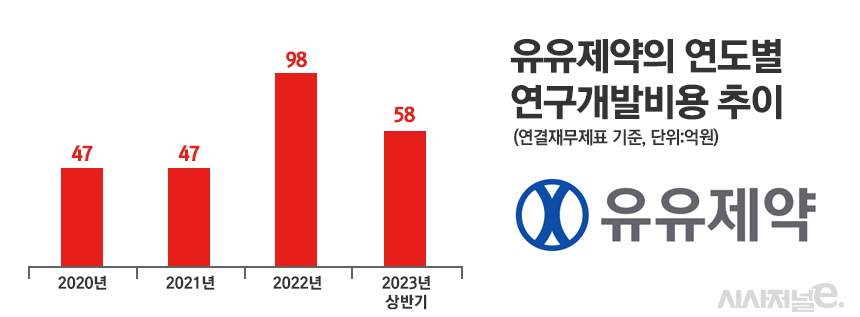
구체적으로 업계는 안구건조증이 발생하는 원인이나 증상이 천차만별이고 개별 환자마다 치료제 효과가 다르게 나온다고 설명한다. 치료제 효과를 수치로 객관화하는 것도 쉽지 않은 작업으로 알려졌다. 이처럼 개발이 어려운 안구건조증 치료제 임상을 지속하는 것은 신중하게 결정해야 한다는 것이 업계 지적이다. 현실적으로 임상비용 부담도 만만치 않은 과제다. 실제 유유제약은 미국 내 7개 병원에서 257명 환자를 대상으로 YP-P10 임상 1/2상 시험을 진행했다. 지난 2021년 연구개발비용으로 47억원(매출의 5.1%)을 투자한 유유제약이 2022년 98억원(9.2%)에 이어 올 상반기 58억원(11.18%)을 집행한 데에는 YP-P10의 미국 임상비용이 적지 않은 비중을 차지했기 때문으로 풀이된다.
제약업계 관계자 A씨는 “안구건조증 치료제 임상은 미국에서 진행하는 경우가 많은데 비용이 적지 않게 필요해 부담이 큰 편”이라며 “일단 개발을 보류한 것은 긍정적”이라고 말했다. 이에 유유제약은 향후 R&D 핵심을 탈모 치료제에 맞추기로 했다. 지난 2019년부터 연구를 진행해왔던 ‘YY-DUT’ 프로젝트를 가동할 예정인 것이다. 구체적으로 GSK의 두타스테리드 성분 탈모 치료제 ‘아보다트’에 비해 1/3 축소된 크기의 개량신약 개발을 추진하는 계획이다. 기존 오리지널 품목 크기를 줄였기 때문에 환자 복용 편의성이 향상될 것이라는 회사측 설명이다.
두타스테리드 성분은 남성호르몬인 테스토스테론이 탈모를 유발하는 DHT 호르몬으로 변화하도록 작용하는 5알파 환원효소 Type-Ⅰ 및 Type-Ⅱ 모두를 억제하는 탈모 치료 작용기전을 갖고 있다. 즉 탈모 환자가 두다스테리드 성분 의약품을 복용하면 DHT 호르몬이 생성되지 않아 테스토스테론이 체내 축적되고 탈모 진행 방해 효과가 있다는 것이다. 이에 ‘피나스테리드’ 성분과 함께 탈모 치료제 핵심 성분으로 꼽힌다.
특히 유유제약은 미국과 유럽의 탈모 치료제 시장을 겨냥해 ‘YY-DUT’ 프로젝트를 가동할 방침이다. 유유제약 관계자는 “아보다트는 미국과 유럽에서 탈모가 아닌 전립선 치료제 적응증을 갖고 있다”며 “현지에서는 피나스테리드 성분 탈모 치료제가 사용된다”고 말했다. Data Bridge Market Research에 따르면 북미 탈모 치료제 시장은 2021년 기준 18억 3935만 달러 규모로 평가됐다. 연평균성장률이 5.9%를 기록, 오는 2029년 29억 960만 달러에 달할 것으로 예상된다. 유럽 탈모 치료제 시장은 6.1% 연평균성장률로 2027년 13억 9061만 달러에 달할 것으로 보고됐다.
유유제약은 2024년 미국과 유럽에서 임상에 돌입, 2026년 현지 탈모 치료제 시장에 출시한다는 계획이다. 회사는 최근 스페인 바르셀로나에서 개최된 ‘CPHI Worldwide 2023’에 참가해 YY-DUT 프로젝트를 홍보한 바 있다. 제약업계 관계자 B씨는 “국내에서 다수 업체가 탈모 치료제 개발을 진행하고 있는데 이중 일부는 개량신약이고 일부는 신약 초기 단계”라며 “유유제약의 경우 임상을 무난하게 마무리할 경우 목표로 하는 미국과 유럽에서 두타스테리드 성분 탈모 치료제로 허가 받는 것이 중요하다”고 말했다.
결국 안구건조증 치료제에서 탈모 치료제 개발로 방향을 전환한 유유제약은 향후 적지 않은 난제가 예상된다. 국내외 다수 개발 업체 중 유유가 어떤 경쟁력을 확보할지 주목된다. 제약업계 관계자 C씨는 “유유제약은 상대적으로 높은 성공율 등 여러 요소를 분석해 개량신약 개발을 결정한 것으로 보인다”며 “미국과 유럽 현지에서 임상을 시작할 예정인만큼 현지화 전략으로 임상을 진행해야 한다”고 조언했다.
