퇴행성 질환 황반변성, 고령화 따라 관련 시장 성장 전망
아일리아, 안구 내 1~3개월 마다 반복주사로 투약 부담 커
경구용·점안액·피하주사 방식까지···새 투약방식 개발
[시사저널e=김지원 기자]국내 바이오 기업이 황반변성 신약 개발에 나서고 있다. 안구 내 직접 주사로 투약 부담이 큰 현 치료제 대신, 먹는 형태의 알약이나 점안액을 선보인다는 목표다. 새로운 투약형태와 작용기전을 지닌 신약을 선보여 편의성을 개선하고, 14조원에 달하는 황반변성 시장을 조준한다.
28일 제약·바이오 업계에 따르면 케어젠, 넥스세라, 니오테스바이오, 베노바이오, 큐라클, 뉴라클제네틱스 등이 황반변성 신약 연구 개발을 진행 중이다. 황반변성은 눈 안쪽 망막 중앙부위인 황반에 발생하는 변성으로, 시력 저하를 유발하는 퇴행성 질환이다. 75~84세 인구의 약 30%에서 발병되는 대표적인 노인성 질환으로, 방치할 경우 실명에 이를 수 있다.
인구 고령화에 따라 황반변성 환자는 증가할 것으로 예상된다. 이에 업계는 황반변성 치료제 시장 규모가 지난해 105억2000만달러(약 14조원) 규모에서 2030년 179억달러(약 23조원) 규모로 성장할 것이라고 전망한다.
◇글로벌 블록버스터 치료제 '아일리아'
현 황반변성 치료제로는 지난해 글로벌 매출 12조원을 기록한 블록버스터 ‘아일리아’가 있지만, 안구 내에 직접 주사해야 한다는 점에서 투약 부담이 크다. 황반변성 발병에는 안구 내 염증과 혈관내피세포성장인자(VEGF)가 중요한 역할을 하는 것으로 알려져 있다.
아일리아는 VEGF를 억제하는 방식으로, 안구에 신생혈관 생성을 막는 약물을 주사해 시력을 담당하는 황반 퇴화를 늦추는 기전이다. 다만 눈에 반복적으로 1~3개월마다 직접 투여해야하는 데 따른 부담이 있다.
이에 국내 바이오 업계는 투약 편의성 개선에 초점을 맞췄다. 반복 투여 부담을 줄이거나, 경구용 알약이나 점안액으로 투여방식을 차별화할 계획이다.
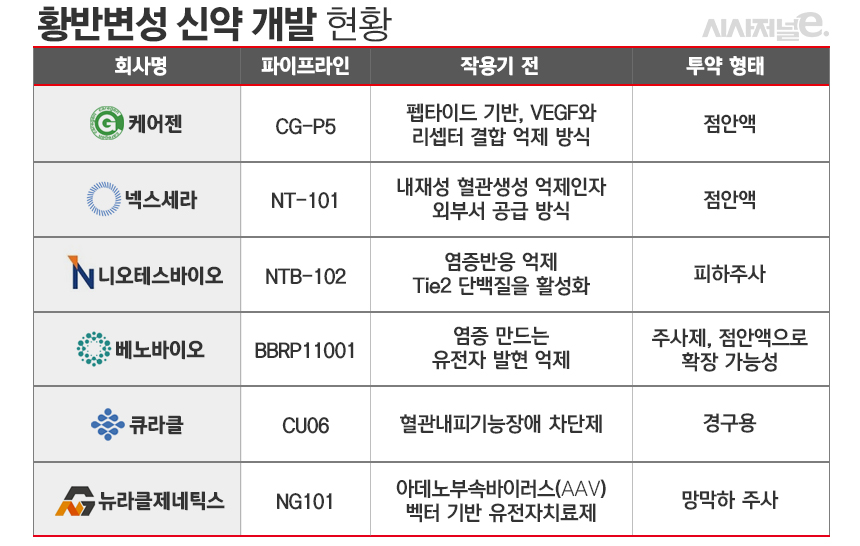
◇투약 편의성 강화한 케어젠·넥스세라···"점안액 형태 신약개발"
케어젠은 황반변성 신약후보물질 ‘CG-P5’의 미국 임상 1상 환자 투약을 완료했다고 지난 27일 밝혔다. 케어젠이 개발한 CG-P5는 합성 펩타이드로, 생체조건 내에서 혈관내피 성장인자 수용체(VEGFR-2)와 결합해 맥락막 신생혈관 생성을 억제하는 기전이다. 즉 VEGF 수용체를 타깃으로, VEGF와 수용체가 결합하는 것을 막아 신생혈관 생성을 억제하는 것이다. 투여 방식은 점안액 형태다.
케어젠 이번 임상은 45명 모두 습성 황반변성 증상이 있는 대상으로 하며, 임상에 사용하는 약물 농도는 30mg 단일 농도를 적용했다. 아일리아 치료군을 양성 대조군으로 두고 결과를 서로 비교하는 형식이다.
케어젠 관계자는 “단일농도로 임상이 진행되고 있는 만큼, 진행에 오랜 기간이 걸리지 않을 것”이라며 “한 참가자 별로 3개월간 치료를 진행한다”고 밝혔다.
이어 “점안액 형태의 CG-P5 투여군과 아일리아 투여군의 결과를 1개월마다 비교가능할 전망”이라며 “최종 보고서가 나오기 전에도 중간 결과를 비교해볼 수 있을 것”이라고 덧붙였다.
넥스세라는 점안형 약물로 습성 황반변성 치료제 후보물질 ‘NT-101’을 개발 중이다. NT-101은 내재성 혈관생성 억제인자를 외부에서 공급하는 방식이란 점에서 기존 VEGF 억제 방식과 차별점을 갖는다. 이에 따라 부작용 없이 장기간 사용이 가능하며, 기존 치료제에 반응하지 않거나 내성이 생긴 환자도 치료효능이 있다. 넥스세라는 오는 2024년 중 미국에서 습성 황반변성 점안형 치료제 NT-101의 임상을 시작한단 목표다.
◇니오테스바이오·베노바이오 “기존 치료제 미충족 수요 해결”
니오테스바이오는 항체 치료제 NTB-102를 개발 중이다. NTB-102는 망막질환을 일으키는 주요 물질 중 하나인 ‘Ang2’를 치료용 물질로 전환시키는 항체로, 염증 반응을 억제하는 동시에 Tie2 단백질을 활성화시키는 기전이다. 망막내 불완전한 혈관을 정상화시키고 망막 내 저산소증을 해결함으로써 기존 VEGF 저해제가 가진 미충족 수요를 해결할 수 있다.
베노바이오는 ‘BBRP11001’의 개발을 진행할 예정이다. BBRP11001은 기존 항체의약품 치료제 대비 황반변성에 대한 근본적인 치료가 가능하다는 설명이다.
베노바이오 관계자는 “기존 VEGF만 억제하는 기전과 달리, BBRP11001은 염증관련 유전자를 억제하는 방식”이라며 “염증을 만드는 유전자 발현을 조절한다”고 밝혔다.
이어 그는 “유전자 발현을 막는 것으로, 혈관생성이라든과 염증 등 관련한 부분을 모두 상위에서 통제할 수 있다”고 덧붙였다. 다만 현재까지 투여방법은 아일리아와 동일하다.
그는 “BBRP11001의 분자량 자체가 작은 만큼, 약물 효력 확인 이후에는 점안제 형태로 접근하는 것을 고려 중”이라고 설명했다. 현재 호주에서 임상 1상 승인신청계획서(IND)를 제출한 상태다.
◇경구용으로 장기투여 가능한 큐라클·치료 유전자 넣은 뉴라클제네틱스
큐라클은 경구용 치료제 CU06의 임상 2a상의 탑라인을 내년 상반기 중 발표할 예정이다. CU06는 최초 경구용 혈관내피기능장애 차단제(Endothelial Dysfunction Blocker)로, 신생혈관 억제 외에 망막 내 모세혈관에서 발생하는 혈관내피기능장애를 정상화해 망막 혈관질환을 치료한다.
큐라클 관계자는 “기존의 항VEGF 치료제는 모두 주사제”라며 “경구용 치료제는 주사제 대비 복용 편의성 및 안전성을 제공해 장기적 투여가 가능하다”고 밝혔다. 아울러 그는 “CU06의 차별화된 작용기전으로, 항 VEGF가 듣지 않는 환자에게도 적용가능하다”며 “망막 혈관질환 환자 중 약 40%는 VEGF 작용이 효과가 없는데, 이들에게 새로운 대안이 되어줄 것으로 기대한다”고 강조했다.
뉴라클제네틱스는 습성 노인성 황반변성 신약후보물질인 ‘NG101’의 캐나다 임상 1·2a상을 진행 중이다. ‘NG101은 아데노부속바이러스(AAV) 벡터(전달체)를 기반으로 개발된 유전자치료제다.
뉴라클제네틱스 관계자는 “치료 유전자를 몸 안에 넣는 방식”이라며 “기존 치료제가 항-VEGF 단백질을 눈에 투여한다면, NG101은 항-VEGF 단백질을 계속 만들어 내는 유전자를 몸 안에 넣어, 지속해서 해당 단백질을 만들어주는 작용을 하도록 했다”고 설명했다.
투여방식은 '망막하 주사'다. 그는 “망막 밑에 조그맣게 구멍을 뚫어 치료 유전자를 넣는 것”이라며 “수술이 필요하지만 1회로 끝나며, 당일 퇴원이 가능하다”고 덧붙였다.
