동아ST, 상반기 627억원 R&D 집행···매출 대비 R&D 비중은 19.6%
스텔라라 시밀러 DMB-3115 임상 연내 완료 예정···내년 9월 미국 출시 추진

[시사저널e=이상구 의약전문기자] 올 초 중개연구 전문가를 영입한 동아ST가 상반기 R&D(연구개발) 비용을 27% 늘렸다. 이처럼 R&D에 적극성을 띤 동아ST가 내년 9월로 예정된 ‘스텔라라’ 바이오시밀러(복제약)의 미국 출시 후 어떤 실적을 올릴 지 주목된다.
7일 관련업계에 따르면 동아ST가 지난 2월 영입한 박재홍 사장이 근무 7개월을 맞았다. 1969년생 박 사장은 연세대 생명공학과와 동대학원에서 각각 학사와 석사 학위를 받은 후 미국 보스턴대학교 의과대학에서 박사 학위를 수여 받았다. 그는 글로벌 제약사 얀센과 다케다, 베링거인겔하임에서 중개연구 전문가로서 혁신 신약개발을 이끌어왔다. 중개연구란 기초연구 결과가 임상연구에 잘 구현되도록 하는 것을 지칭한다.
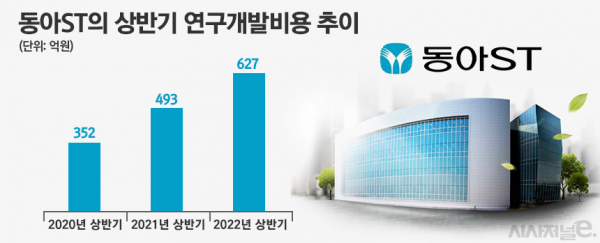
박 사장이 동아ST에서 근무한 기간 동안 여러 변화가 있었지만 일단 R&D비 급증이 눈에 띈다. 반기보고서에 따르면 동아ST는 연결재무제표 기준, 올 상반기 627억원을 R&D에 집행했다. 지난해 상반기 493억원에 비해 27.4% 증가한 규모다. 매출 대비 R&D 비중은 19.6%다. 참고로 동아ST는 상반기 125억원 영업이익을 올려 전년대비 42.7% 성장했다. 제약업계 관계자는 “동아ST의 매출 대비 R&D 비중이 20%에 육박한 것에 의미를 부여할 수 있다”며 “상반기 실적을 공개한 제약사 중 19.6% 비중은 10위권 안에 드는 실적이며 현실적으로 쉽지 않은 수치”라고 말했다.
동아ST는 이같은 R&D비를 바이오시밀러와 신약 등 현재 개발을 진행 중인 품목에 집행한 것으로 분석된다. 우선적으로 회사 R&D에서 주목되는 내용은 스텔라라 바이오시밀러 ‘DMB-3115’다. 스텔라라는 얀센이 개발한 인터루킨(IL)-12, 23 억제제 계열 자가면역질환 치료제다. 건선과 건선성 관절염, 크론병, 궤양성 대장염 등을 치료할 때 활용된다. 의약품 시장조사기관 아이큐비아 글로벌 데이터에 따르면 지난해 기준, 전 세계 스텔라라 매출은 141억달러다. 지난 2020년 269억원이던 스텔라라 국내 매출은 지난해 34.2% 증가한 361억원을 달성했다. 이어 올 1분기 매출은 101억원으로 전년대비 33.7% 증가했다. 제약업계 관계자는 “스텔라라 매출이 지난해 처음으로 300억원을 돌파했다”라며 “후발 약제가 다수 나왔지만 건선에서 건선성 관절염, 크론병, 궤양성대장염 등으로 적응증을 꾸준히 확대한 스텔라라가 시장에서 긍정적 반응을 얻고 있다“고 설명했다.
동아ST는 지난해 4월 DMB-3115 임상 3상에 진입했다. 같은 해 11월 605명 환자 모집을 완료했다. 이어 회사는 연내 DMB-3115 임상 3상을 완료할 예정이다. 키움증권도 DMB-3115 임상 3상이 올해 말 종료돼 내년 초 결과를 발표할 것으로 전망한 바 있다. 당초 DMB-3115는 동아쏘시오홀딩스와 메이지세이카파마가 지난 2013년부터 공동 개발해 왔던 품목이다. 2020년 7월 효율적 프로젝트 수행을 위해 동아쏘시오홀딩스에서 동아ST로 개발과 상업화 권리가 이전된 것이다. 이후 현재는 동아ST와 메이지세이카파마가 공동 개발하고 있다. 동아ST와 메이지세이카파마는 글로벌 상업화 준비도 완료한 상태다. 두 기업은 지난해 7월 글로벌 제약사 인타스와 DMB-3115 기술수출 계약을 체결하고 인타스에 한국과 일본, 일부 아시아 국가를 제외한 글로벌 지역 허가와 판매 권리를 양도한 바 있다.
스텔라라 물질 특허 만료일이 미국에서 2023년 9월, 유럽 2024년 7월 만료됨에 따라 동아ST도 해당 시기에 맞춰 DMB-3115를 상업화할 계획이다. 제약업계 관계자는 “스텔라라 바이오시밀러를 개발하는 제약사는 미국 암젠과 독일 포미콘, 아일랜드 알보텍, 일본 후지, 중국 바이오테라솔루션, 호주 누클론, 한국 삼성바이오에피스, 셀트리온 등 다수”라며 “오는 2023년 9월 미국에서 바이오시밀러 제품이 출시되며 본격 경쟁이 진행될 것”으로 예상했다. 또 다른 제약업계 관계자는 “제약사들은 최소한 올해 말까지는 임상시험을 마치고 결과 분석을 해야 내년 9월 전 미국 FDA(식품의약국) 판매허가를 받아 바이오시밀러 출시를 진행할 수 있다”고 말했다.
동아ST는 신약 개발에도 주력하는 상태다. 우선 과민성방광 치료제 ‘DA-8010’은 국내 임상 2상에서 유효성과 안정성, 복용편의성을 입증했다. 회사는 지난 3월 595명 환자를 대상으로 DA-8010 임상 3상을 시작했다. 키움증권은 DA-8010이 오는 2024년 임상 3상이 종료돼 이듬해인 2025년 출시될 것으로 예상했다. 동아ST는 ‘슈가논’에 이어 당뇨병 치료제 ‘DA-1241’도 개발하고 있다. 미국 임상 1b상에서 혈당강하 효과를 확인한 데 이어 현재 글로벌 임상 2상을 준비 중이다. 이밖에도 회사는 주 1회 패치형 치매 치료제로 개발하는 ‘DA-5207’의 국내 임상 1b상을 진행하고 있다.
결국 글로벌제약사에서 활동하던 중개연구 전문가를 올 초 영입한 동아ST는 전년대비 27% 늘어난 금액을 투자하는 등 R&D에 적극적 모습을 보이고 있다. 이같은 움직임 성과는 1년 후 미국에서 구체적으로 나올 것으로 예상돼 스텔라라 바이오시밀러 임상시험 추이에 관심이 집중될 전망이다. 제약업계 관계자는 “모든 사업 시초는 사람에서 나오는데 실적을 올리려면 기본적으로 사람에 대한 투자가 중요하다”며 “지난해 영업이익이 부진했던 동아ST 상반기 실적 호전과 R&D는 큰 의미에서 연결된 구조로 보인다”고 말했다.
