파멥신, '올린베시맙' 단독투여 임상 중단···임상 난항 원인
머크와 공동임상 2건은 그대로 진행···“선택과 집중 불가피"
글로벌 네트워크 구축에 집중···기술이전·협력 논의 활발
[시사저널e=염현아 기자] 국내 바이오업체 파멥신이 현재 개발 중인 핵심 파이프라인의 주요 임상시험을 중단했다. 코로나19 펜데믹으로 원료의약품 및 임상 비용이 급증한 데다, 임상이 지연되면서 개발의 어려움을 겪자, 결국 선택과 집중을 택한 것이다. 다만 파멥신은 최근 글로벌 바이오 행사에 연달아 초청된 만큼, 국내외 기업들과의 협력으로 돌파구를 마련하겠다는 전략이다.
19일 국내 바이오업계에 따르면 항암 치료제 '올린베시맙'을 집중 개발 중인 파멥신이 최근 주요 임상시험을 잠정 중단했다. 해당 임상은 로슈의 '아바스틴' 치료 후 재발한 뇌종양 환자를 대상으로, 미국과 호주에서 2a상을 진행 중이었다.
악성 뇌종양인 교모세포종은 재발 시 생존율이 6개월 미만으로 예후가 좋지 않다. 몸 속 정상 세포는 건드리지 않고 암세포만 골라 죽이는 ‘아바스틴’이란 표적항암제가 쓰이고 있지만, 효과는 제한적이다. 치료 6개월 후 약물에 내성이 생긴다는 게 아바스틴의 최대 단점이다.
이에 파멥신은 다양한 종류의 고형암을 적응증으로 하는 항-신생혈관형성 항체치료제 '올린베시맙'을 개발해, 표적항암제의 부작용을 겪은 환자들을 위해 단독투여 임상을 진행해왔다. 다만 팬데믹으로 임상 비용이 늘어나고, 환자 모집에 어려움이 지속되자 중단을 택한 것이다.
2019년 말 미국 스탠포드·플로리다 올랜도 암센터, 호주 멜버른의 올리비아뉴튼죤 암센터에서 시작한 임상 2a상은 올 2월 초까지 8명의 환자가 모집됐고, 이후 코로나19 재유행으로 환자 모집 지연이 본격화됐다.
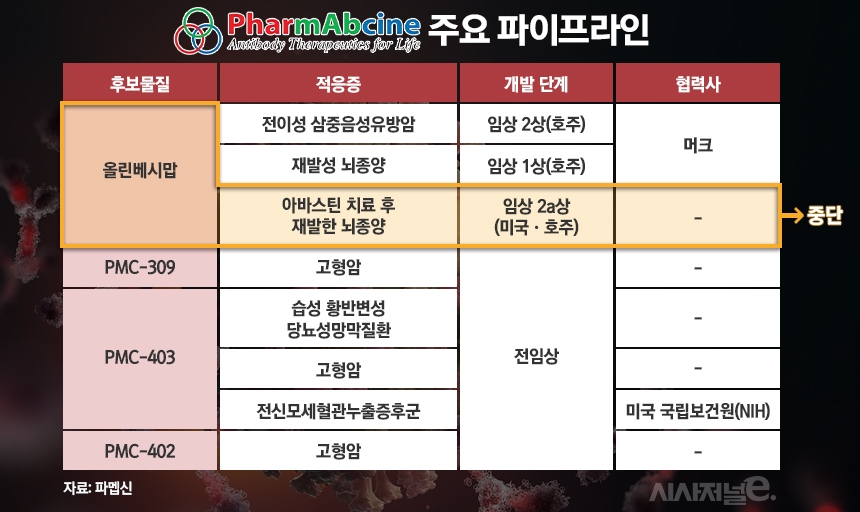
다만 파멥신은 미국 머크(MSD)와 공동 진행 중인 병용 임상은 그대로 진행한다는 계획이다.
파멥신은 지난해 4월 머크와 전이성 삼중음성유방암 치료제 개발을 위한 공동임상 연구협약을 맺고, 12월 임상 2상에 진입했다. 호주에서 전이성 삼중음성유방암 환자 36명을 대상으로 머크의 '키트루다(펨브롤리주맙)'와 올린베시맙을 병용 투여해 효과를 확인하는 방식이다. 재발성 뇌종양에 대한 병용 임상 1b상은 지난해 말 투여를 완료해, 2상 진입 시기를 검토하고 있다.
파멥신 관계자는 "올린베시맙은 파멥신의 주력 파이프라인인 만큼, 세 개의 임상을 모두 완주해 개발 성공이 목표였지만, 현재로선 많은 제약이 따르는 상황"이라며 "개발 성공 가능성이 높은 파이프라인을 선택·집중해 가속화하는 쪽을 택했다"고 설명했다. 다만 이 관계자는 "이번에 잠정 중단이 결정된 올린베시맙의 단독투여 임상은 향후에 재개할 가능성도 있다"고 덧붙였다.
결국 비용 부담으로 핵심 파이프라인을 축소하게 된 파멥신은 글로벌 네트워크를 통해 기술이전 및 협력을 강화하는 모양새다. 파멥신은 올 초 'JP모건 헬스케어 컨퍼런스'에 이어 지난달 '제프리스 헬스케어 컨퍼런스', '바이오 인터네셔널 컨벤션(바이오 USA)' 등 여러 국제 행사에 초청됐다.
올해로 6년 연속 바이오USA에 참석해온 파멥신은 3년 만에 대면으로 열린 올해 행사에선 'Presenting Company(발표 기업)'로 선정돼 올린베시맙을 소개하고, 새로운 투자자 발굴에 나섰다.
올해 바이오USA에 참석한 한 업계 관계자는 "국제 무대의 '프로참석러'로 통하는 파멥신은 머크와의 MOU(업무협약)도 글로벌 컨퍼런스에서 체결됐다"며 "특히 글로벌 블록버스터 항암제인 아바스틴을 대체할 치료제 개발에 전 세계 기업들의 관심이 높은 만큼, 해당 파이프라인은 기술이전이나 공동임상으로 이어나갈 것으로 보인다"고 전했다.
파멥신에 따르면, 현재 전임상 단계에 있는 'PMC-309'와 'PMC-403'은 빠르면 올 연말 1상에 대한 임상시험계획(IND)을 신청한다는 계획이다. 국가신약개발사업 지원과제로 연구개발(R&D) 지원을 받은 고형암 치료제 PMC-309에 대한 기술이전 논의도 현재 진행 중이다.
