SD바이오·씨젠, 내년 성장동력 부재·사업성 악화 우려 잠식
오미크론발 코로나19 제품 문의 쇄도···공급량 맞추기 총력
양사 “코로나19 진단제품 추가 개발 및 상용화 준비 박차”
[시사저널e=최다은 기자] 국내 진단키트 업체 SD바이오센서와 씨젠이 Non-Covid 제품 다각화를 예고했으나, 정작 업계에서는 지난해와 올해에 이어 내년에도 양사의 실적은 Covid 제품이 견인할 것이란 평가가 나온다. 오미크론발 코로나19 상황이 악화일로로 치닫자, SD바이오센서와 씨젠의 주력 연구개발(R&D) 및 영업 제품이 다시 Covid 부문으로 맞춰지고 있는 모양새다.
23일 업계에 따르면 지난 11월 씨젠과 SD바이오센서는 “Non-Covid 제품에 대한 대규모 R&D 투자를 단행한다”며 “해외 법인을 통해 현지 Non-Covid 제품 공급망을 확보하고 R&D 투자를 늘려 내년도 성장 동력 저하 우려를 타개하겠다”고 밝혔다. Non-Covid 포트폴리오 다각화를 모색해 코로나19 제품으로 집중된 매출 비중을 줄이겠다는 전략이다.
그러나 전 세계적 오미크론 변이 확산과 돌파감염이 폭증하면서, 양사는 다시 Covid 제품 생산 및 국내외 공급에 주력하는 모습이다. 이 때문에 성장 동력 부재와 사업성 악화 우려가 무색해졌다는 평가가 나온다. 매출 대부분도 Covid 제품 위주로 발생될 것이라 전망된다.
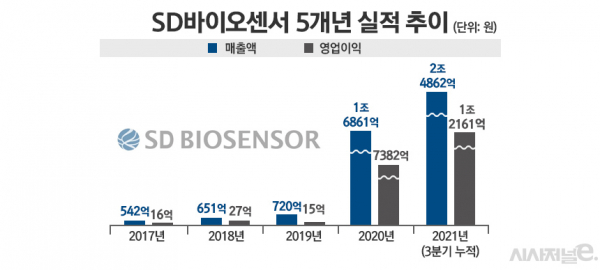
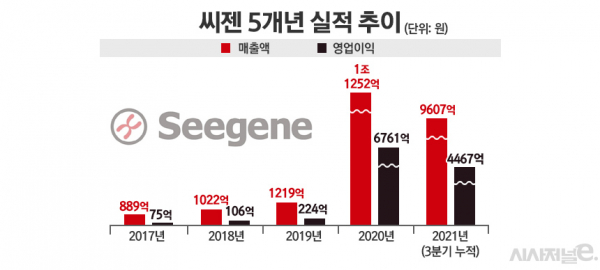
금융감독원 전자공시시스템에 따르면 지난 2019년 SD바이오센서의 매출은 730억원에 불과했으나, 코로나19 팬데믹 발생 이후인 지난해엔 1조6862억원의 매출을 세우며 1년 만에 1조 클럽에 진입했다. 씨젠의 실적도 코로나19 수혜를 제대로 누렸다. 지난 2019년 1219억원대였던 씨젠의 매출은 지난해 1조1252억원을 기록하며 900% 이상 성장했다.
SD바이오센서의 영업이익은 지난 2019년 15억원에서 지난해 7382억원, 씨젠은 같은 기간 224억원에서 6761억원으로 각각 약 4900%, 2900% 수익성이 대폭 개선됐다. SD바이오센서와 씨젠의 올 3분기 누적 매출은 각각 2조4862억원 9607억원을 달성했다. 영업이익은 각각 1조2161억원, 4667억원을 기록했다.
◇ SD바이오·씨젠, 코로나19 진단제품 추가 개발 및 공급 총력
SD바이오센서와 씨젠은 오미크론발 전 세계적 코로나19 감염 폭증세에 당분간은 Covid 제품 파이프라인 확대에 집중하겠다는 계획이다. 양사는 기존 코로나19 진단제품 수출 판로를 바탕으로 국내외 공급량을 늘려 늘어나는 수요에 대응할 방침이다.
지난 22일 SD바이오센서는 식품의약품안전처(식약처)로부터 현장분자진단 카트리지 ‘STANDARD M10 SARS-CoV-2’ 정식허가를 획득해, 국내 판매를 위한 절차에 돌입할 것으로 보인다. 해당 제품은 이미 지난 8월부터 해외로 공급이 시작된 바 있다. 유전자 추출부터 증폭까지 30~60분 내 검사가 가능하며, 기존 PCR 검사의 정확도는 유지하되 1시간 이내에 결과 확인이 가능한 현장분자진단기기다.
또 SD바이오센서는 오미크론 변이를 구별할 수 있는 분자진단 PCR 시약과 M10 카트리지를 연내 개발 완료해 상용화 준비에 돌입할 계획이다. 국내외에서 오미크론 변이를 구별할 수 있는 진단시약 수요가 높아지고 있는 가운데, 빠르면 내년 상반기 공급을 계획하고 있다. 내년에도 오미크론 확산세가 지속될 것으로 보여 시장성 확보가 가능할 것이란 판단이다.
SD바이오센서 관계자는 “오미크론발 코로나19 상황이 국내외적으로 더욱 악화되는 양상을 보이면서, Covid 관련 제품 수요가 폭증하고 있다”며 “지난달까지만해도 업계에서 수익성 악화에 대한 우려가 커졌는데 한달 만에 기조가 바뀌었다”고 말했다. 그러면서 “기존 코로나19 진단제품과 최근 식약처 허가를 받은 M10의 경우 빠르면 내년 상반기부터 국내 공급이 시작될 것으로 보인다”고 덧붙었다.
씨젠은 지난 19일 유럽의 코로나19 재확산에 따른 진단시약 수요 증가 대응을 위해 280만명분의 코로나19 진단시약을 전세기로 유럽에 공급했다. 앞서 씨젠은 지난해 4월에도 이스라엘에 전세기를 통해 코로나19 진단시약을 수출한 바 있다. 오미크론 확산 이후 국내외 코로나19 관련 제품 수요가 폭발적으로 증가하고 있는 가운데, 이전부터 씨젠의 주요 Covid 제품 공급국이었던 유럽에서의 수요가 대폭 늘었다는 설명이다.
또 씨젠은 오미크론 변이 감염자만을 별도로 구분할 수 있는 진단시약 개발을 완료해 상용화를 위한 준비에 들어갔다. 씨젠은 지난 1일 본지와 통화에서 “오미크론 변이 감염자만을 별도로 구분할 수 있는 진단시약 개발에 대한 내부 검토에 들어갔다”고 밝힌 바 있다.
씨젠 관계자는 “코로나19 상황이 최소 내년까지는 이어질 것이란 판단하에 Covid 관련 추가 제품 개발과 상용화 준비에 박차를 가하고 있다”며 “씨젠은 Covid뿐만 아니라 수십가지의 Non-Covid 제품도 보유하고 있긴 하지만, 현재 코로나19 제품 수요가 국내외로 쇄도하면서 공급물량을 맞추는데 전사적 역량을 집중하고 있다”고 설명했다. 이어 “유럽에서만 판매 중인 코로나19 진단시약 ‘Allplex™ SARS-CoV-2 Master Assay’에 대해서도 국내 수요가 계속될 경우, 국내 공급을 위한 상용화 준비를 계획하고 있다”고 밝혔다.
